TECNOLOGÍA FARMACÉUTICA III
DOBLE GRADO EN BIOTECNOLOGÍA Y EN FARMACIA
Curso 2023/2024
1. Datos de la asignatura
(Fecha última modificación: 06-06-23 13:24)- Código
- 100136
- Plan
- 2020
- ECTS
- 4
- Carácter
- Curso
- 4
- Periodicidad
- Segundo cuatrimestre
- Idioma
- ESPAÑOL
- Área
- FARMACIA Y TECNOLOGÍA FARMACÉUTICA
- Departamento
- Ciencias Farmacéuticas
- Plataforma Virtual
Campus Virtual de la Universidad de Salamanca
https://studium.usal.es/
Datos del profesorado
- Coordinador/Coordinadora
- Hinojal Zazo Gómez
- Grupo/s
- 1
- Centro
- Fac. Farmacia
- Departamento
- Ciencias Farmacéuticas
- Área
- Farmacia y Tecnología Farmacéutica
- Despacho
- Farmacia y Tecnología Farmacéutica (Sótano de la Facultad)
- Horario de tutorías
- M, X, J de 9 a 11 h
- URL Web
- https://produccioncientifica.usal.es/investigadores/107727/detalle
- hinojal@usal.es
- Teléfono
- 923294500 ext 6743
- Profesor/Profesora
- Cristina Maderuelo Martín
- Grupo/s
- 1
- Centro
- Fac. Farmacia
- Departamento
- Ciencias Farmacéuticas
- Área
- Farmacia y Tecnología Farmacéutica
- Despacho
- Sótano
- Horario de tutorías
- L, V de 11 a 14 h
- URL Web
- https://produccioncientifica.usal.es/investigadores/57180/detalle
- cmaderuelo@usal.es
- Teléfono
- 677584149 Ext 6742
- Profesor/Profesora
- Aránzazu Zarzuelo Castañeda
- Grupo/s
- 1
- Centro
- Fac. Farmacia
- Departamento
- Ciencias Farmacéuticas
- Área
- Farmacia y Tecnología Farmacéutica
- Despacho
- Sótano
- Horario de tutorías
- M, X, J de 9 a 11 h
- URL Web
- https://produccioncientifica.usal.es/investigadores/55914/detalle
- drury@usal.es
- Teléfono
- 923 294 500 Ext.6761
2. Sentido de la materia en el plan de estudios
Bloque formativo al que pertenece la materia.
Tecnología Farmacéutica I, Tecnología Farmacéutica II y Tecnología Farmacéutica III
Papel de la asignatura.
En esta asignatura se imparten conocimientos relacionados con las Normas de Correcta Fabricación (NCF ó GMP) de medicamentos de origen químico y biológico, tanto a nivel industrial como a nivel hospitalario y en la Oficina de Farmacia, así como conocimientos sobre normas de Buenas Prácticas de Laboratorio (BPL ó GLP) y protocolos de estudio.
Perfil profesional.
Interés de la materia para una profesión futura.
Especialistas en medicamentos con conocimiento de los distintos requisitos exigidos para la fabricación de los mismos siguiendo la normativa vigente.
3. Recomendaciones previas
ASIGNATURAS QUE SE RECOMIENDA HABER CURSADO
Se recomienda que el alumno haya cursado previamente la asignatura de Tecnología Farmacéutica I ya que ello proporciona los conocimientos teóricos y prácticos previos sobre los procesos tecnológicos de elaboración de medicamentos, lo que ayuda a comprender determinados aspectos de las Normas de Correcta Fabricación.
ASIGNATURAS QUE SE RECOMIENDA CURSAR SIMULTÁNEAMENTE
Tecnología Farmacéutica II
4. Objetivo de la asignatura
Formar profesionales en la cultura de la calidad. Comprender y manejar las Normas de Correcta Fabricación. Formar profesionales capaces de integrarse en la industria químico-farmacéutica y cosmética.
5. Contenidos
Teoría.
DESCRIPTORES
Garantía de calidad. Normas de Correcta Fabricación. Procedimientos Normalizados de Trabajo. Buenas Prácticas de Laboratorio.
CONTENIDOS TEÓRICOS
Tema 1.- Garantía de Calidad. Sus tres pilares básicos: Normas de Correcta Fabricación, Buenas Prácticas de Laboratorio y Buenas Prácticas Clínicas. Diferencia entre Garantía de Calidad y Control de Calidad.
Tema 2.- Normas de Correcta Fabricación relativas a Personal. Organización del personal.
Tema 3.- Procedimientos Normalizados de Trabajo (PNT). Partes de que consta un PNT. Tipos de PNTs.
Tema 4.- Normas de Correcta Fabricación relativas a las Instalaciones. Características que deben cumplir. Zonas de fabricación. Zonas de almacenamiento. Zonas de control de calidad. Zonas auxiliares.
Tema 5.- Maquinaria y Utillaje. Segregación y espacio de servidumbre. Etiquetaje y documentación relativa a la maquinaria. Mantenimiento y limpieza.
Tema 6.- Validación. Cualificación de Diseño, cualificación de la instalación, cualificación operacional, cualificación del proceso. Plan máster de validación.
Tema 7.- Validación de métodos analíticos de acuerdo a normas ICH y FDA.
Tema 8.- Documentación relativa a las materias primas y material de acondicionamiento. Recepción. Cuarentena. Proveedores. Homologación de proveedores. Calidad concertada. Almacenamiento de producto terminado.
Tema 9.- Documentación relativa a la Fabricación: Guías de fabricación. Fórmula patrón y método patrón. Controles en proceso.
Tema 10.- Normas de Higiene. Importancia de las mismas. Vestimenta, y comportamiento en zonas de ambiente controlado. Contaminación cruzada.
Tema 11.- Zonas de ambiente controlado. Requisitos ambientales en la fabricación de medicamentos estériles y no estériles. Concepto y requisitos de salas limpias
Tema 12.- Buenas Prácticas de Laboratorio (BPL, GLP). Personal. Documentación propia de las BPL. Certificación BPL.
Tema 13.- Normas de correcta fabricación específicas para medicamentos de Terapia Avanzada (ATMPs). Generalidades de ATMPs. Diferencias con las NCF de medicamentos de síntesis química.
Práctica.
CONTENIDOS PRÁCTICOS
Práctica 1.- Validación de un método analítico.
Práctica 2.- Redacción de un Procedimiento Normalizado de Trabajo.
Práctica 3.- Realización de una simulación de autoinspección.
SEMINARIOS
Seminario 1.- Organigrama del laboratorio de elaboración de medicamentos individualizados de una oficina de farmacia.
Seminario 2.- Diseño una planta de producción de medicamentos para uso humano
Seminario 3.- Calibración y cualificación de equipamiento.
Seminario 4.- Especificaciones de materiales de partida.
Seminario 5- Comportamiento del personal en una sala limpia de clase A.
TUTORIAS ESPECIALIZADAS
Se reforzarán conocimientos y conceptos con material audiovisual sobre fabricación de medicamentos siguiendo Normas de Correcta Fabricación y normas de higiene, utilizando la enseñanza "on line" a través de studium.
ACTIVIDADES ACADÉMICAS DIRIGIDAS
Se programarán visitas a Laboratorios Farmacéuticos como actividad práctica complementaria. La realización de la visita y el número de alumnos que podrán participar en la misma está supeditado a las facilidades y disponibilidad de la Industria Farmacéutica.
6. Competencias a adquirir
Básicas / Generales.
CB2 - Que los estudiantes sepan aplicar sus conocimientos a su trabajo o vocación de una forma profesional y posean las competencias que suelen demostrarse por medio de la elaboración y defensa de argumentos y la resolución de problemas dentro de su área de estudio
CB3 - Que los estudiantes tengan la capacidad de reunir e interpretar datos relevantes (normalmente dentro de su área de estudio) para emitir juicios que incluyan una reflexión sobre temas relevantes de índole social, científica o ética.
CB4 - Que los estudiantes puedan transmitir información, ideas, problemas y soluciones a un público tanto especializado como no especializado.
CB5 - Que los estudiantes hayan desarrollado aquellas habilidades de aprendizaje necesarias para emprender estudios posteriores con un alto grado de autonomía.
Específicas.
CE1 - Identificar, diseñar, obtener, analizar, controlar y producir fármacos y medicamentos, así como otros productos y materias primas de interés sanitario de uso humano o veterinario.
CE3 - Saber aplicar el método científico y adquirir habilidades en el manejo de la legislación, fuentes de información, bibliografía, elaboración de protocolos y demás aspectos que se consideran necesarios para el diseño y evaluación crítica de ensayos preclínicos y clínicos.
CE4 - Diseñar, preparar, suministrar y dispensar medicamentos y otros productos de interés sanitario
CE7 - Identificar, evaluar y valorar los problemas relacionados con fármacos y medicamentos, así como participar en las actividades de Farmacovigilancia.
CEM4-1 - Diseñar, optimizar y elaborar las formas farmacéuticas garantizando su calidad, incluyendo la formulación y control de calidad de medicamentos, el desarrollo de fórmulas magistrales y preparados oficinales.
CEM4-2 - Aplicar el control de calidad de productos sanitarios, dermofarmacéuticos y cosméticos y materiales de acondicionamiento.
CEM4-7 - Conocer las operaciones básicas y procesos tecnológicos relacionados con la elaboración y control de medicamentos.
Transversales.
Instrumentales:
- Capacidad para aplicar los conocimientos a la práctica
- Toma de decisiones
- Habilidades de gestión de la información
- Comunicación oral y escrita
Personales:
- Trabajo en equipo
- Capacidad crítica y autocrítica
Sistemáticas:
- Capacidad de aprender
7. Metodologías
- Clases teóricas.
- Clases prácticas en grupos reducidos.
- Seminarios sobre diversos aspectos de la asignatura.
- Enseñanza virtual de algunos aspectos de la asignatura (plataforma Studium)
- Visita a un laboratorio farmacéutico.
8. Previsión de Técnicas (Estrategias) Docentes
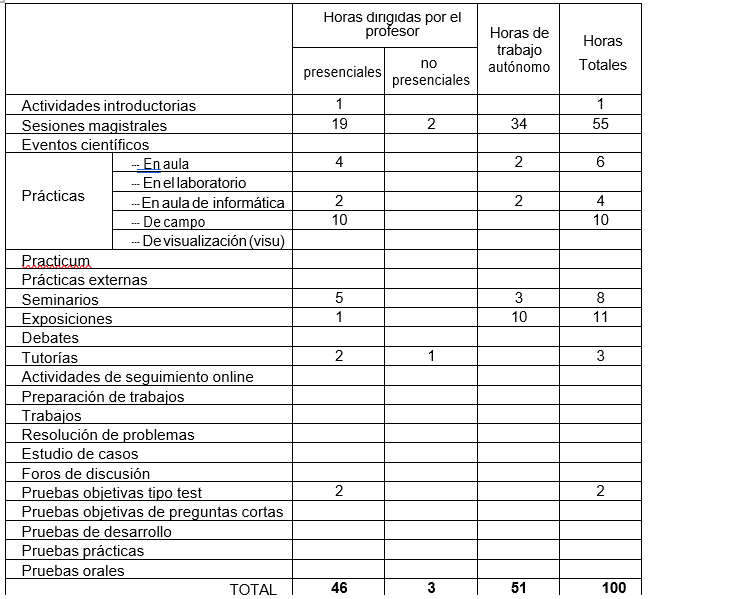
9. Recursos
Libros de consulta para el alumno.
LIBROS
- RAMÓN COMPAÑÓ BELTRÁN Y ÁNGEL RIOS CASTRO. Garantía de la calidad en los laboratorios analíticos. Síntesis. Madrid. 2002.
- ENRIQUE BENÉITEZ PALOMEQUE. –1995- Good manufacturing practices. La gestión técnica en la fabricación de medicamentos. Consejos Prácticos. Centro de Estudios Superiores de la Industria Farmacéutica. Madrid.
- FRANCISCO JAVIER GARCÍA GARCÍA. Validación de métodos analíticos. 2001
- GRAHAM C. COLE. Instalaciones de Producción Farmacéutica. Diseño y aplicaciones. 2002
- JUAN SABATER TOBELLA Y ANTONIO VILUMARA TORRALLARDONA. Buenas prácticas de laboratorio (GLP) y Garantía de Calidad (Quality Assurance): Principios básicos. Diaz de Santos. Madrid. 1988.
LIBROS DE CONSULTA PARA EL ALUMNO
- RAMÓN SALAZAR MACIÁN. Gestión de la calidad en el desarrollo y fabricación industrial de medicamentos. Tomo I. Desarrollo farmacéutico. Barcelona. 2001.
- RAMÓN SALAZAR MACIÁN. Gestión de la calidad en el desarrollo y fabricación industrial de medicamentos. Tomo II. Fabricación Industrial. Barcelona. 2001.
- RAMÓN SALAZAR MACIÁN. Cualificación y validación: elementos básicos de la calidad y productividad. Barcelona. 2007.
Otras referencias bibliográficas, electrónicas o cualquier otro tipo de recurso.
- Guía de Normas de Correcta Fabricación de la Unión Europea para Medicamentos de uso humano y uso veterinario. Agencia Española de Medicamentos y Productos Sanitarios – AEMPS [Internet] Disponible en: https://www.aemps.gob.es/industria/inspeccionNCF/guiaNCF/home.htm
- Directiva 2003/94/CE de la Comisión, de 8 de octubre de 2003, por la que se establecen los principios y directrices de las prácticas correctas de fabricación de los medicamentos de uso humano y de los medicamentos en investigación de uso humano.
- Directiva 91/412/CEE. Directiva por la que se establecen los principios y directrices de las Normas de Correcta Fabricación para los medicamentos de uso veterinario
- Real Farmacopea Española. Quinta Edición, Ministerio de Sanidad y Consumo. Madrid. 2015
- The European Pharmacopoeia. 10.8th Edition. Strasbourg. Council of Europe, 2022.
- Plataforma STUDIUM en la que se recogen las presentaciones que se proyectan en las clases teóricas, enlaces de interés, test de autoevaluación y noticias e información relacionadas con el contenido de la asignatura.
10. Evaluación
Consideraciones generales.
Clases practicas
La realización de las clases prácticas es obligatoria en el grupo en que es convocado el alumno, siendo un requisito imprescindible para poder superar la asignatura.
Evaluación continua:
Participación activa y entrega de actividades en clases de teoría, seminarios, prácticas y exposiciones.
Examen escrito:
Se realizará un examen escrito sobre el contenido de las clases magistrales, de las clases prácticas, de los seminarios y de la información que se hubiera proporcionado a lo largo del periodo docente.
El examen contendrá preguntas tipo test multirrespuesta.
Criterios de evaluación.
Se realizará un proceso de Evaluación continua que contribuirá en un 40% a la calificación final y que tendrá en cuenta los siguientes aspectos:
- Exposición y defensa póster (10%)
- Realización y participación activa en las prácticas (15%)
- Participación activa en aula y seminarios (15%)
Por último, se realizará una prueba escrita para evaluar la asimilación de conocimientos teóricos cuya calificación contribuirá a la nota global en un 60%. La prueba será un test multirrespuesta.
Será imprescindible para poder superar la asignatura:
- obtener al menos un 5 (sobre 10) en la prueba escrita.
- obtener un 5 (sobre 10) tras la suma de todas las calificaciones de las actividades evaluables (seminarios, póster, prácticas, y prueba escrita).
Instrumentos de evaluación.
- Prueba escrita (CB2,5; CE1,3,4,7; CEM4-1,2,7)
- Evaluación de las prácticas ((CB3; CE3; CEM4-2; C. Transversales)
- Evaluación de seminarios ((CB3, 4; CE3,4; CEM4-1,2; C. Transversales)
- Participación y asistencia (C. Transversales)
METODOLOGÍAS DE EVALUACIÓN
La calificación global se obtendrá sumando las calificaciones de los distintos apartados evaluados según los siguientes criterios de calificación:
- Examen*: 60% de la calificación total
- Póster (exposición / defensa): 10% de la calificación total
- Practicas: 15% de la calificación total
- Participación activa seminarios: 15% de la calificación total
- Bonificación en la nota final: asistencia y actividades complementarias y/o notas destacadas
*Sobre el contenido de las clases teóricas/seminarios y prácticas.
Recomendaciones para la evaluación.
Participación activa en las clases teóricas, prácticas y seminarios.
Recomendaciones para la recuperación.
Será imprescindible para poder superar la asignatura en la convocatoria extraordinaria:
- obtener al menos un 5 (sobre 10) en la prueba escrita.
- obtener un 5 (sobre 10) tras la suma de todas las calificaciones de las actividades evaluables (seminarios, póster, prácticas, y prueba escrita).


