PRODUCCIÓN INDUSTRIAL DE MEDICAMENTOS
GRADO EN FARMACIA
Curso 2020/2021
1. Datos de la asignatura
(Fecha última modificación: 16-07-20 9:19)- Código
- 100167
- Plan
- 201
- ECTS
- 5.00
- Carácter
- OPTATIVA
- Curso
- 5
- Periodicidad
- Primer cuatrimestre
- Idioma
- ESPAÑOL
- Área
- FARMACIA Y TECNOLOGÍA FARMACÉUTICA
- Departamento
- Ciencias Farmacéuticas
- Plataforma Virtual
Datos del profesorado
- Profesor/Profesora
- Cristina Maderuelo Martín
- Grupo/s
- 1
- Centro
- Fac. Farmacia
- Departamento
- Ciencias Farmacéuticas
- Área
- Farmacia y Tecnología Farmacéutica
- Despacho
- Sótano
- Horario de tutorías
- Lunes, miércoles y viernes 10 a 11 h.
- URL Web
- https://produccioncientifica.usal.es/investigadores/57180/detalle
- cmaderuelo@usal.es
- Teléfono
- 923 294500. Ext 6742
- Profesor/Profesora
- Amparo Sánchez Navarro
- Grupo/s
- 1
- Centro
- Fac. Farmacia
- Departamento
- Ciencias Farmacéuticas
- Área
- Farmacia y Tecnología Farmacéutica
- Despacho
- Ubicado en planta sótano de Facultad Farmacia
- Horario de tutorías
- Lunes a Jueves de 10 a 11 h
- URL Web
- https://produccioncientifica.usal.es/investigadores/56100/detalle
- asn@usal.es
- Teléfono
- 923 29 45 00. Ext.6744
2. Sentido de la materia en el plan de estudios
Bloque formativo al que pertenece la materia.
Modulo 9. Optativas
Conjunto de asignaturas vinculadas entre sí: Tecnología Farmacéutica I, II y III
Papel de la asignatura.
Esta asignatura ofrece una visión general del funcionamiento y estructura de la industria
farmacéutica y el papel profesional del farmacéutico en la misma.
Una vez estudiada la tecnología de producción de formas farmacéuticas y las Normas de Correcta Fabricación, se completa la visión del estudiante sobre este sector a través de los contenidos ofrecidos en esta asignatura. Se abordará el funcionamiento de un laboratorio fabricante de medicamentos desde la llegada de las materias primas a las instalaciones hasta la salida del producto terminado, pasando por la elaboración, control, instalaciones disponibles, etc.
Perfil profesional.
Se imparte formación básica necesaria para integrarse profesionalmente en el ámbito de la industria farmacéutica, cosmética y veterinaria.
Los contenidos ofrecidos constituyen una introducción a la especialidad de Gestión y Producción en la Industria Farmacéutica del Máster adscrito a esta facultad que lleva por título Evaluación y Desarrollo de Medicamentos.
3. Recomendaciones previas
Asignaturas que se recomienda haber cursado: Tecnología Farmacéutica I, II y III
4. Objetivo de la asignatura
OBJETIVOS GENERALES:
- Dar una visión global de la estructura y funcionamiento de la industria farmacéutica.
- Establecer las bases para el acceso como profesional cualificado al ámbito de la industria farmacéutica.
- Promover el análisis crítico en la evaluación de problemas y toma de decisiones
OBJETIVOS ESPECÍFICOS:
- Proporcionar conocimientos sobre las etapas y aspectos técnicos relacionados con la producción industrial de medicamentos
- Introducir al alumno en la terminología propia de la producción industrial de medicamentos
- Formar al alumno para el conocimiento de los criterios básicos del diseño de plantas farmacéuticas
- Capacitar al alumno para integrarse en los equipos de trabajo relacionados con las diferentes operaciones técnicas propias de una planta de fabricación
5. Contenidos
Teoría.
BLOQUE 1. INTRODUCCIÓN A LA INDUSTRIA FARMACÉUTICA
Tema 1. La industria farmacéutica. Definición y características del sector farmacéutico. Estructura y objetivos. Evolución y situación actual. I+D+i farmacéutico. Outsourcing. Estructura y diseño de una planta farmacéutica.
BLOQUE 2. ÁREAS Y SERVICIOS
Tema 2. Sistemas de producción de agua. Métodos de tratamiento del agua. Especificaciones técnicas en el diseño de sistemas de tratamiento de agua.
Tema 3. Sistemas de tratamiento de aire. Filtración del aire. Especificaciones técnicas en el diseño de sistemas de tratamiento de aire.
BLOQUE 3. ÁREA INDUSTRIAL Y OPERACIONES TÉCNICAS DE UNA PLANTA DE FABRICACIÓN
Tema 4. Materias primas farmacéuticas. Documentación técnica de las sustancias activas. ICHQ7a/ Parte II NCF-UE. Suministro, recepción y almacenamiento.
Tema 5. Producción. Operaciones del área industrial. Documentación de fabricación. Planificación de la producción. Herramientas informáticas para la gestión de la producción.
Tema 6. Acondicionamiento. Operaciones y documentación de acondicionamiento. Líneas de acondicionamiento; diseño. Fallos y repercusión.
Tema 7. Control de calidad. Métodos analíticos. Especificaciones. Tratamiento de las desviaciones. Certificado de análisis. Seguimiento de lotes..
Tema 8. Muestreo en la industria farmacéutica
Tema 9. Garantía de calidad. Liberación de lotes. Incidencias, desviaciones y OOS. Cualificaciones y validaciones. Análisis de riesgos. Control de cambios. Auditorias. Reclamaciones y devoluciones. Retiradas del mercado.
BLOQUE 4. INDUSTRIALIZACIÓN DE PROCESOS
Tema 10. Plantas piloto. Desarrollo farmacéutico y cambio de escala. Calidad por diseño.
Tema 11. Aspectos técnicos en el registro de medicamentos. Contenido del expediente de registro (CTD)
Tema 12. Industrialización de nuevos sistemas terapéuticos. Problemática de las formulaciones innovadoras.
SEMINARIOS
- Charla divulgativa a cargo de un profesional del sector de materias primas
- Charla divulgativa a cargo de un profesional del sector de producto farmacéutico
- Charla divulgativa a cargo de un profesional del sector de ingeniería de salas
- Charla divulgativa a cargo de un profesional de garantía de calidad
- Informe de desarrollo farmacéutico en formato CTD (Common Technical Document)
- Salidas profesionales del farmacéutico dentro de la Industria Farmacéutica
Práctica.
- Validación de un proceso de fabricación teórico. Análisis de riesgos
- Caso práctico: análisis de patentes
- Caso práctico: planificación de la fabricación
- Visita a un laboratorio farmacéutico
6. Competencias a adquirir
Básicas / Generales.
− Adquirir capacidad crítica para resolver problemas y tomar decisiones con iniciativa
− Capacidad de aplicar los conocimientos a la práctica
− Capacidad de expresarse correctamente y con precisión estructurando correctamente el contenido
− Trabajo en equipo
Específicas.
− Comprender la estructura y funcionamiento de la industria farmacéutica
− Conocer y comprender la gestión y características propias de la asistencia farmacéutica en el ámbito de la industria farmacéutica (CEM5-16)
− Adquirir conocimientos sobre los criterios técnicos/farmacéuticos en el diseño de plantas industriales
− Conocer, manejar y evaluar la documentación técnica asociada a los procesos de desarrollo y elaboración de medicamentos
− Conocer y participar en las operaciones técnicas de los procesos de producción de medicamentos
− Contribuir a la resolución de problemas durante las etapas de producción de medicamentos a nivel industrial
− Desempeñar su actividad profesional en el entorno de la industria farmacéutica
− Asumir el papel del farmacéutico en la industria farmacéutica y afines
− Conocer y aplicar con precisión la terminología propia de la industria farmacéutica
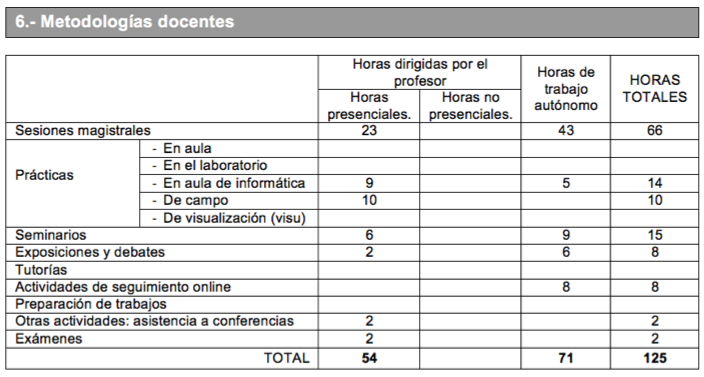
7. Metodologías
8. Previsión de Técnicas (Estrategias) Docentes
9. Recursos
Libros de consulta para el alumno.
-
Martínez Pacheco R. Tratado de Tecnología Farmacéutica. Volumen I, II y III: Ed. Sintesis, Madrid, 2016
-
Walkiria S. Schlindwein and Mark Gibson, Pharmaceutical Quality by Design: A Practical Approach, John Wiley & Sons Ltd. 2018. DOI:10.1002/9781118895238
-
Salazar MR, Gestión de la calidad en el desarrollo y fabricación industrial de medicamentos, Vol. I y II, Ed. Salazar, 1999.
- Cole GC, Instalaciones de producción farmacéutica. Diseño y aplicaciones, Traducción autorizada por la editorial Taylor y Francis. GEA consultoría Editorial, Madrid, 2002.
- Macián, R.S., Gestión de la calidad en el desarrollo y fabricación industrial de medicamentos: fabricación industrial. Vol. I y II, Ed. Salazar, 2001
- Levin M.(ed.). Pharmaceutical process scale-up. 3rd ed. New York: Informa Healthcare, cop. 2011
- Gad, S.C., Pharmaceutical Manufacturing Handbook: Production and Processes. 2008: Wiley.
- Normas sobre medicamentos de la Unión Europea. Madrid.: Ministerio de Sanidad y Consumo. Secretaría General Técnica. Centro de Publicaciones; 2002. vol. 4: Normas de correcta fabricación: medicamentos de uso humano y medicamentos veterinarios.
- Real Farmacopea Española. Quinta Edición, Ministerio de Sanidad y Consumo. Madrid. 2015
- The European Pharmacopoeia. 10th Edition. Strasbourg. Council of Europe, 2020.
- USP 43–NF 38. Rockville. The United States Pharmacopeial Convention, 2020.
Otras referencias bibliográficas, electrónicas o cualquier otro tipo de recurso.
Revistas electrónicas:
- Chemical Engineering Science
- Journal of Controlled Release
- Pharmaceutical Processing
- Pharmaceutical Programming
- Pharmaceutical Technology Europe
Webs:
- Agencia Española de Medicamentos y productos sanitarios: www.aemps.gob.es/
- Agencia Europea de Medicamentos (EMA): http://www.ema.europa.eu/
- Asociación Española de Farmacéuticos de la Industria: http://www.aefi.org/
- Food and Drug Administration (FDA): http://www.fda.gov/
- The International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use: http://www.ich.org/home.html
10. Evaluación
Consideraciones generales.
Con el objetivo de evaluar los conocimientos y competencias adquiridas, el alumnado tendrá que realizar:
• Realizar trabajo en equipo durante la realización de las prácticas dentro de los grupos convocados durante el curso
• Realizar los seminarios dentro de los grupos convocados durante el curso
• Participación activa en las clases teóricas y prácticas
• Participación activa en seminarios y visitas programadas
Criterios de evaluación.
Se aplicarán los siguientes criterios de evaluación:
Dominio de los contenidos teóricos y prácticos
Manejo con precisión de conceptos en las diferentes actividades de evaluación
Estructura, presentación y claridad en la realización de las diferentes pruebas de evaluación
Expresión oral y escrita correcta y precisa en la realización de las pruebas de evaluación
Participación activa en las clases teóricas y prácticas, individualmente y en los grupos de trabajo
Para superar la asignatura será necesario obtener una calificación global igual o superior a cinco. Esta calificación global se obtendrá calculando la media ponderada según los siguientes criterios de calificación, siendo necesario aprobar cada una de las partes:
1. Examen*: 65% de la calificación total
2. Practicas: 15% de la calificación total
3. Seminarios: 15% de la calificación total
4. Participación activa en las clases magistrales y seminarios: 5% de la calificación total.
5. Bonificación en la nota final: actividades complementarias y/o notas destacadas
*Sobre el contenido de las clases teóricas/seminarios y prácticas. Podrá contener preguntas tipo test multi-respuesta, problemas, preguntas cortas y cuestiones que impliquen la aplicación de los conceptos impartidos en la asignatura
Instrumentos de evaluación.
- Prueba escrita (CE001-7)
- Evaluación de las prácticas (CE001-7)
- Evaluación de seminarios (CT001-2)
- Participación en clase y asistencia
Recomendaciones para la evaluación.
Asistencia a clase y participación activa
Realización adecuada de las clases prácticas
Asistencia y aprovechamiento de las visitas programadas
Realización de los trabajos de seminarios
Resolución de dudas a través de foros o preguntas en la plataforma Studium
Recomendaciones para la recuperación.
El alumno deberá realizar un examen de la parte o partes no superadas y alcanzar una nota mínima de 5 en todas y cada una de ellas para superar la evaluación


